Questões de Vestibular
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 991 questões
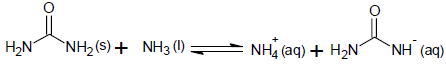
Sobre a natureza das interações entre as espécies envolvidas na reação, o comportamento químico das substâncias reagentes e o átomo de nitrogênio, é correto afirmar:

De acordo com as informações contidas na tabela sobre as
propriedades físicas das substâncias listadas, é correto afirmar:
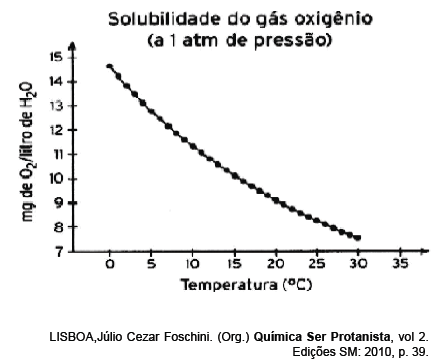
O comportamento do gás oxigênio com a variação de temperatura
descrito no gráfico, bem como o comportamento físico geral dos
gases, permitem afirmar corretamente que
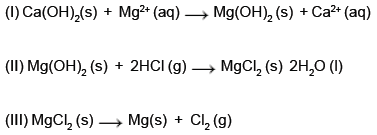
A partir das reações representadas e das propriedades dos elementos e substâncias, é correto afirmar:
C6H12O6 → 2 C2H5 OH + 2 CO2
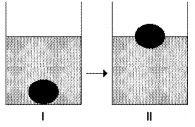
Para determinar a ação destes fungos, muitas pessoas, após prepararem a massa utilizando fermento biológico, separam uma porção dela em forma de “bola” e a mergulham num recipiente com água, aguardando que ela flutue, como pode ser observado, respectivamente, em I e II do esquema a seguir:
Já o fermento químico, é formado basicamente por bicarbonato de sódio, que se decompõe termicamente de acordo com a seguinte equação:
NaHCO3 → Na2 CO3 + H2 O + CO2
Com relação à utilização dos dois tipos de fermentos, é incorreto afirmar que:
Cada tipo de planta cresce melhor em solos com faixa específica de pH. Os valores de pH do solo se devem à solução intersticial presente, ou seja, a água presente no solo e seus respectivos solutos. A tabela abaixo fornece a faixa de “pH ótimo” para algumas plantas, o que facilita a produtividade de flores e frutos.
Dada a reação, assinale a afirmativa correta:

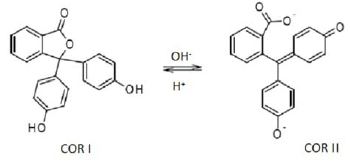
Sobre esses dados é correto afirmar que

Em frascos de água oxigenada, a concentração dessa é expressa em volumes, como água oxigenada a 10 volumes, a 20 volumes etc. Essa concentração corresponde ao número de litros de gás oxigênio medido nas condições normais de temperatura e pressão (CNTP), obtidos pela decomposição completa de todo H2O2 em um litro de solução. Considerando que a reação abaixo transcorra na CNTP e que R = 0,082 atm.L.mol-1K-1, assinale o que for correto.
 1 H2O(l) + 1/2 O2(g)
1 H2O(l) + 1/2 O2(g)


Em países de inverno rigoroso, lagos e rios congelam-se na superfície e a água de máxima densidade encontra-se no fundo a 4 ºC. Esse fato é de fundamental importância para a preservação da vida aquática. Outro fenômeno comum de lugares frios é a formação de finas camadas de gelo nas ruas e nas estradas. Para abrandar os danos causados por esse gelo depositado, os moradores costumam jogar sal (NaCl) sobre o gelo. Considerando as afirmações acima e os dados de que a constante molal de diminuição do ponto de congelamento da água (Kc) é 1,9 e que 0 ºC e 100 ºC correspondem a 32 ºF e 212 ºF, respectivamente, assinale o que for correto.


Em países de inverno rigoroso, lagos e rios congelam-se na superfície e a água de máxima densidade encontra-se no fundo a 4 ºC. Esse fato é de fundamental importância para a preservação da vida aquática. Outro fenômeno comum de lugares frios é a formação de finas camadas de gelo nas ruas e nas estradas. Para abrandar os danos causados por esse gelo depositado, os moradores costumam jogar sal (NaCl) sobre o gelo. Considerando as afirmações acima e os dados de que a constante molal de diminuição do ponto de congelamento da água (Kc) é 1,9 e que 0 ºC e 100 ºC correspondem a 32 ºF e 212 ºF, respectivamente, assinale o que for correto.
