Questões de Vestibular de Química - Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess.
Foram encontradas 340 questões
C6H4(OH)2(aq) + H2O2
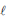 ) hidroquinona
) hidroquinona O calor envolvido nessa transformação pode ser calculado, considerando-se os processos:
C6H4(OH)2(aq) → C6H4O2(aq) + H2(g) ΔHº = + 177 kJ . mol-1
H2O (
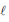 ) + 1/2 O (g) → H2O2 (aq) ΔHº= + 95 kJ .mol-1
) + 1/2 O (g) → H2O2 (aq) ΔHº= + 95 kJ .mol-1
H2O(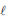 ) → 1/2 O2(g) + H2 (g) ΔHº= + 286 kJ .mol-1
) → 1/2 O2(g) + H2 (g) ΔHº= + 286 kJ .mol-1
I. CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) ΔHo= −212,8kcalmol−1 II. CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
( ) A partir dos métodos do calor de formação e da energia de ligação, obtêm-se os mesmos valores de variação de entalpia da reação expressa na equação química I. ( ) A queima de alcanos só é exotérmica se os produtos forem gasosos. ( ) A reação expressa na equação química II é mais exotérmica que aquela expressa na equação química I. ( ) O calor da reação expressa na equação química II equivale à soma do calor de vaporização da água com o calor envolvido na reação expressa na equação química I.
A alternativa que contém a sequência correta, de cima para baixo, é a
Sob certas condições, tanto o gás flúor quanto o gás cloro
podem reagir com hidrogênio gasoso, formando,
respectivamente, os haletos de hidrogênio HF e HCl,
gasosos. Pode-se estimar a variação de entalpia 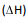 de cada
uma dessas reações, utilizando-se dados de energia de
ligação. A tabela apresenta os valores de energia de ligação
dos reagentes e produtos dessas reações a 25 ºC e 1 atm.
de cada
uma dessas reações, utilizando-se dados de energia de
ligação. A tabela apresenta os valores de energia de ligação
dos reagentes e produtos dessas reações a 25 ºC e 1 atm.

Com base nesses dados, um estudante calculou a variação
de entalpia 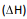 de cada uma das reações e concluiu,
corretamente, que, nas condições empregadas,
de cada uma das reações e concluiu,
corretamente, que, nas condições empregadas,
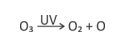
O gráfico representa a energia potencial de ligação entre um dos átomos de oxigênio que constitui a molécula de O3 e os outros dois, como função da distância de separação r.
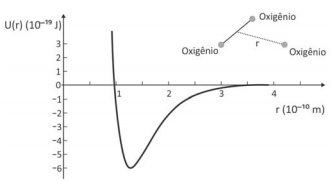
A frequência dos fótons da luz ultravioleta que corresponde à energia de quebra de uma ligação da molécula de ozônio para formar uma molécula de O2 e um átomo de oxigênio é, aproximadamente .
A equação química que representa a reação que ocorre na fermentação alcoólica da glicose é
C6H12O6(aq) → 2 C2H6O(aq) + 2 CO2(g) ΔrH = ?
Assinale a alternativa que apresenta o valor correto da entalpia padrão da reação (ΔrH) de fermentação da glicose, em kJ/mol.
Entalpias de formação em kJ/mol
Substância ΔfH C6H12O6(aq) – 1 277 C2H6O (aq) – 278 CO2(g) – 394
O poder calorífico de um gás liquefeito é conhecido como a quantidade de energia liberada pela sua queima. Se o poder calorífico do propano é cerca de 50 kJ/g, assinale a alternativa que apresenta, corretamente, o volume, em m3 , de propano que deve ser queimado para liberar 1,0×103 kJ de energia, à temperatura de 20 ◦C e 1 atmosfera.
Dados: Massa molar do propano = 44,1 g/mol
Pode-se concluir corretamente que, na combustão completa de 1 mol desse hidrocarboneto, as quantidades de matéria, e CO2 e de H2O produzidas são, em mol, respectivamente, iguais a
Entre os gráficos 1, 2 e 3, aquele que representa corretamente a reação da fosfina com o oxigênio, descrita no texto, é o
Leia o texto para responder a questão.
De onde vem o cheiro de carro novo?
De acordo com o gerente de uma montadora de veículos, o cheiro é composto por uma combinação de vários tipos de substâncias químicas usadas na fabricação do veículo, incluindo solventes, plásticos, colas, tecidos e borracha. Porém, muitas delas são altamente tóxicas, porque contêm Compostos Orgânicos Voláteis (COVs) em sua composição, como benzeno, tolueno e formol, que podem ser letais dependendo da quantidade. Eles acabam escapando e impregnando o ar, porque não requerem altas temperaturas para evaporarem.
<http://tinyurl.com/y8ucob6c> Acesso em: 13.11.2017. Adaptado.
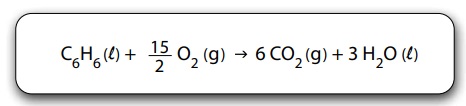
A entalpia de combustão do benzeno pode ser determinada conhecendo-se os valores das entalpias de formação do gás carbônico, assim como da água e do benzeno líquidos.
A tabela apresenta os valores de entalpia de formação de algumas substâncias nas condições padrão.
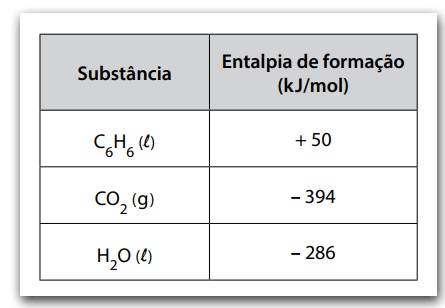
A entalpia de combustão completa do benzeno, em kJ/mol, é
O besouro-bombardeiro consegue afastar seus predadores, lançando sobre eles um jato quente e repelente de quinona, substância produzida em seu abdômen, através da reação química entre hidroquinina e peróxido de hidrogênio. O fenômeno pode ser representado pela equação:
C6 H6 O2(aq) + H2O2(aq) → C6 H4O2(aq) + 2H2 O ∆H = –204 kJ/mol
Hidroquinona Quinona
Este composto também pode ser preparado a partir de uma reação de esterificação:
CH3 –CH2 –OH (l) + CH3 –COOH (l) CH3 ⇌ COOCH2 –CH3 (l) + H2O (l)
Para calcularmos a variação de entalpia da reação, ∆H, podemos aplicar a lei de Hess às equações de combustão dos compostos orgânicos presentes na reação de esterificação, apresentadas a seguir.
I. CH3–CH2 –OH (l) + 3 O2 (g) ⇾ 2 CO2 (g) + 3 H2O (l) ∆H = – 1 368 kJ II. CH3COOH (l) + 2 O2 (g) ⇾ 2 CO2 (g) + 2 H2O (l) ∆H = – 875 kJ III. CH3COOCH2CH3 (l) + 5 O2 (g) ⇾ 4 CO2 (g) + 4 H2O (l) ∆H = – 2 231 kJ
Aplicando a lei mencionada, a variação de entalpia da reação de esterificação descrita será, em kJ, igual a
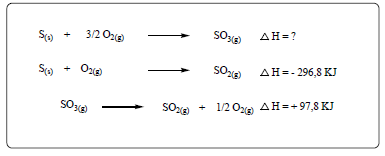
A nitroglicerina - C3H5(NO3)3 – é um nitrato de alquila, descoberta em 1847 por Ascanio Sobrero (químico italiano, 1812-1888), que a obteve misturando glicerina, ácido nítrico e ácido sulfúrico. No estado puro e à temperatura ambiente, a nitroglicerina é um líquido muito explosivo e perigoso. Em 1867, Alfred Nobel (químico sueco, 1833-1896) realizou testes no sentido de melhorar a manipulação da nitroglicerina, misturando-a com materiais inertes, como sílica, pós cerâmicos, argila, gesso, carvão e terras diatomáceas. Esses materiais, agora moldáveis, viriam a se tornar um explosivo muito importante, conhecido como dinamite.
A equação abaixo (não balanceada) representa a reação de decomposição da nitroglicerina:
C3H5(NO3)3(l) → N2(g) + O2(g) + CO2(g) + H2O(g) (não balanceada)
Dados: ∆Hf C3H5(NO3)3(l) = -364 kJ/mol; ∆Hf CO2(g) = -393 kJ/mol; ∆Hf H2O(g)= -242 kJ/mol
De posse das informações, assinale a alternativa que representa a variação de entalpia da reação acima, em kJ por mol de nitroglicerina.
Fazer a mala para uma viagem poderá ser tão simples como pegar algumas latas de spray, que contenham uma mistura de polímero coloidal, para fazer suas próprias roupas “spray-on”. Tanto faz se é uma camiseta ou um traje noturno, o tecido “spray-on” é uma novidade para produzir uma variedade de tecidos leves. A fórmula consiste em fibras curtas interligadas com polímeros e um solvente que produz o tecido em forma líquida. Esse tecido provoca uma sensação fria ao ser pulverizado no corpo, mas adquire a temperatura corporal em poucos segundos. O material é pulverizado diretamente sobre a pele nua de uma pessoa, onde seca quase instantaneamente.

(http://tinyurl.com/qermcv6 Acesso em: 29.08.2014. Adaptado. Original colorido)
A sensação térmica provocada pelo tecido “spray-on”,
quando pulverizado sobre o corpo, ocorre porque o
solvente
A equação química a seguir indica que há participação de gases na reação.
2C (sólido) + O2 (g) −→ 2CO(g)
Considere que, em um primeiro momento, a reação ocorra sem expansão de volume (volume constante) em um sistema fechado a 27 ◦C e que o valor do calor medido seja de 52600 cal.
Se essa mesma reação ocorrer a pressão constante, assinale a alternativa que apresenta, corretamente, o calor liberado, em cal.
(Dado: R = 2 cal/K)
 + 3O2(g) → 2CO2 (g) + 3H2O
+ 3O2(g) → 2CO2 (g) + 3H2O  ΔH = - 1366,8kJ
ΔH = - 1366,8kJ + 25/2 O2(g) → 8 CO2(g) + 9 H2O
+ 25/2 O2(g) → 8 CO2(g) + 9 H2O  ΔH = –5 461,0 kJ
ΔH = –5 461,0 kJDadas as entalpias de formação dos compostos:
CO2(g) ΔHf = - 393 kJ/mol
H2O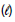 ΔHf = - 286 kJ/mol
ΔHf = - 286 kJ/mol
conclui-se, corretamente, que a entalpia de formação do combustível presente em I é, em kJ/mol,
A2 + B2 → 2 AB
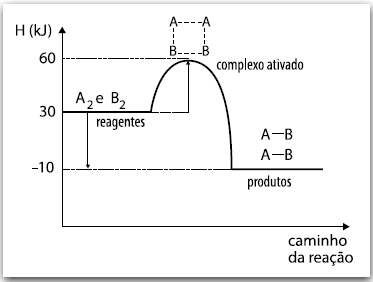
A análise do gráfico permite concluir corretamente que
2 H2(g) + O2(g) → 2 H2O(g) ∆H= - 483,6 kJ
A reação acima é uma reação:
Acerca dessas informações, assinale a alternativa incorreta.
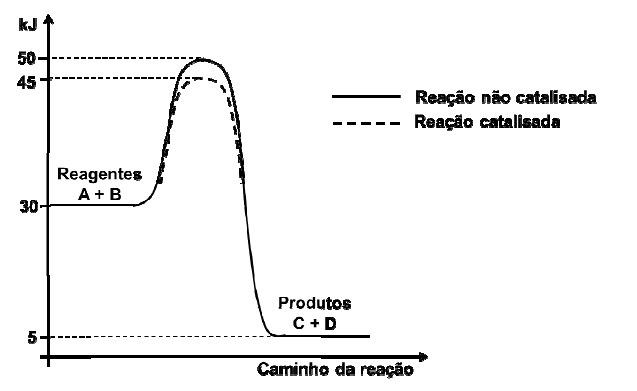
Sobre a reação, podemos afirmar que: