Questões de Concurso
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 2.136 questões
Pesquisadores brasileiros criaram recentemente dois tipos de ossos sintéticos, que poderão ser usados em enxertos nas áreas de medicina e odontologia. Esses novos biomateriais são formados por polímeros e principalmente por nanopartículas minerais de hidroxiapatita, uma cerâmica bioativa que induz o crescimento do tecido ósseo na área do implante.
(Adaptado de: Revista Pesquisa FAPESP, n. 227)
A fórmula da hidroxiapatita sintética é Ca10(PO4)6(OH)2. A porcentagem em massa de oxigênio nesse composto é de
Um analista recebeu amostras de tintura permanente de cabelo da cor “Louro Médio 7.0”, de marcas diferentes, para determinar a quantidade de amônia na composição. Foram utilizadas aproximadamente 3,0 gramas da amostra e diluídas em 50,0 mL de água destilada em balão volumétrico. Em seguida, foram retirados 5,0 mL dessa solução e transferidos para um erlenmeyer de 150,0 mL que continha 50 mL de água destilada. O indicador utilizado foi o verde de bromocresol. A determinação de amônia foi feita por titulação, com uma solução aquosa de ácido clorídrico a 0,1 mol L-1 padronizado.
Os dados da titulação são mostrados na tabela a seguir:
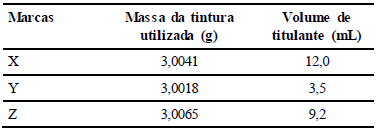
De acordo com a Resolução nº. 79 de 28 de
agosto de 2000 (ANVISA), o teor de amônia deve ser de,
no máximo, 6,0% no produto final. (DADOS: N = 14 g
mol-1
; H =1 g mol-1
; Cl = 35,5 g mol-1
)
ANVISA. Agência Nacional de Vigilância Sanitária. Resolução RDC nº 79, de 28 de agosto de 2000. Estabelece a definição e Classificação de Produtos de Higiene Pessoal, Cosméticos e Perfumes e outros com abrangência neste contexto, 2000. Diário Oficial da União de 31 de agosto de 2000.
De acordo com os resultados obtidos, assinale a
alternativa correta.
Um professor de química ministrou uma aula sobre toxicidade de metais, na qual foi avaliada a inibição do crescimento da raiz de cebola submersa em soluções de sulfato de cobre em diferentes níveis de concentração.
Para o preparo das soluções, foi utilizada uma solução aquosa de sulfato de cobre a 6,2 x 10-5 mol L-1 , e a mesma foi diluída nas proporções de 1:20, 1:10 e 1:1 (v/v). (Dados: Cu = 63,5 g mol-1 ; S = 32,1 g mol-1 ; e O = 16 g mol-1 ).
Sobre o experimento realizado, assinale a
alternativa correta.
Sobre a reação a seguir é CORRETO afirmar:
AsF3(g) + SbF5(l) → [AsF2]+[SbF6]-
(s)
Para padronizar uma solução de ácido clorídrico, um analista pesou 0,764 g de bórax e transferiu quantitativamente para um erlenmeyer, dissolvendo em 50 mL de água destilada. Esta solução foi titulada até coloração rosa com o ácido clorídrico em presença de três gotas do indicador vermelho de metila consumindo 40,00 mL do ácido clorídrico.
A concentração do ácido titulado (em mol.L-1 ) é igual a
Dados: Massa molar do bórax (Na2B4O7.10H2O) = 382g.mol-1
Os sais de nitrato são compostos iônicos muito solúveis em água. Quando se coloca 1 mol de nitrato de cálcio em 1 litro de água ocorre a formação de uma solução na qual os íons estão separados e solvatados por moléculas de água.
Nessa solução, as concentrações em mol.L-1 dos íons cálcio e nitrato, presentes na solução são, respectivamente,
Na preparação de uma curva de calibração para analisar nitrato em amostras de água por meio da técnica de cromatografia iônica, um analista utilizou uma solução padrão de concentração inicial 99,6 mg.L–1 e preparou diferentes volumes de soluções com diferentes concentrações.
A tabela a seguir apresenta volumes utilizados da solução padrão e concentrações das soluções preparadas.
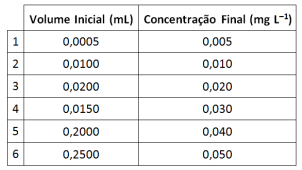
Os maiores volumes (em mL) preparados foram os
correspondentes às soluções
Em 1923, o químico dinamarquês Johannes Brønsted (1879- 1947) e o químico inglês Thomas Lowry (1874-1936) propuseram uma definição de ácidos e bases mais geral do que a proposta anteriormente por Arrhenius (1859-1927).
O conceito de Brønsted- Lowry está baseado no fato de que a reação ácido-base envolve transferência de íons H+ de uma substância para outra.
Analise o equilíbrio a seguir:
HSO3 – (aq)+ H2O(ℓ) ⇄ H2SO3(aq) +OH– (aq)
Baseado nesse conceito, os pares conjugados são:
Para uma determinada pratica em laboratório é necessário o preparo de 200 mL de solução 0,5 mol.L–1 de ácido nítrico a partir de uma solução concentrada desse ácido. A solução concentrada é identificada por: 65%(m/m) e densidade 1,4g.cm–3 .
O volume a ser utilizado dessa solução é de, aproximadamente,
Dados: Massas molares: H = 1g.mol-1 ; N = 14g.mol-1 ; O = 16g.mol-1
A concentração de NaCl é, em mol/L,
A precisão do método é criticamente dependente das propriedades desse composto.
Padrão secundário: substância que tem sua concentração determinada por análise química e é utilizada como referência em análises volumétricas.
O NaOH é um sólido muito higroscópico (absorve umidade do ar), além de reagir com o dióxido de carbono do ar, sendo transformado em carbonato de sódio e água, conforme a equação:
2 NaOH + CO2 Na2-->CO3 + H2O
Com base nessas informações, o hidróxido de sódio é um
É muito comum encontramos álcool no mercado com a indicação: 77oGL.
Gay Lussac (°GL = %V): quantidade em mililitros de álcool absoluto contida em 100 mililitros de mistura hidro-alcoólica.
É comum também, ao lado da concentração em v/v da solução hidro-alcoólica, encontrarmos a indicação INPM.
INPM (%P = porcentagem de álcool em peso ou grau alcoólico INPM): quantidade em gramas de álcool absoluto contida em 100 gramas de mistura hidro-alcoólica. Se quisermos converter 77oGL em INPM, encontraremos o valor:
Dado: densidade do álcool = 0,8 g.cm-3 e da água = 1,0 g.cm-3
Considerando-se a temperatura de 20 ºC, a razão entre a pressão de vapor da acetona pura e a pressão de vapor do removedor de esmalte é, aproximadamente,
Dado Pressão de vapor do acetato de etila: 73 mmHg a 20 ºC Pressão de vapor da acetona: 200 mmHg a 20 ºC M (acetato de etila) = 88,0 g mol-1 M (acetona) = 58,0 g mol-1