Questões de Vestibular
Sobre transformações químicas e energia em química
Foram encontradas 985 questões
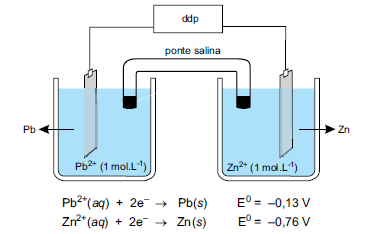
A partir da análise da figura, é correto afirmar que essa pilha tem ddp igual a
Com base nesta informação, podemos afirmar que as substâncias adicionais promoverão:
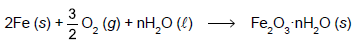
A tabela fornece os potenciais-padrão de redução (Eº) de algumas semirreações, a 25 ºC.

Com base nas informações fornecidas, pode-se afirmar que:
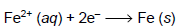
Considerando a Constante de Faraday = 96 500 C/mol, 1 hora = 3 600 s e massa molar do ferro (Fe) = 56 g/mol, a massa aproximada de ferro metálico que pode ser depositada no cátodo, nessas condições, é
CaCℓ2 (s) + H2O (ℓ) → CaCℓ2 (aq) ∆H = −82,7 kJ/mol
Nesse processo,
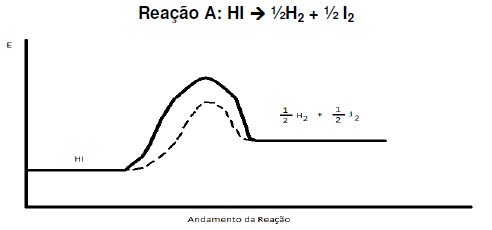
Marque a opção correta:
Observe a equação de formação de etanol a seguir:
2 Cgraf + 3 H2(g) + ½ O2(g) → C2 H6 O(l)
Com base nas equações abaixo que resultam na reação de interesse, calcule o ∆H da reação de formação do etanol.
I. Cgraf + O2(g) → CO2(g) ∆H = -394 kJ/mol
II. H2(g) + ½ O2(g) → H2 O(l) ∆H = -286 kJ/mol
III. C2
H6
O(l) + 3 O2(g) → 2 CO2(g) + 3 H2
O(l) ∆H = -1368 kJ/mol
A tabela mostra valores do pH da água líquida em diferentes temperaturas.
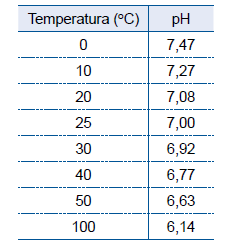
A análise desses dados permite afirmar que o produto iônico da água, Kw,_______ com a elevação da temperatura e que a reação de autoionização da água _______ energia, sendo, portanto, um processo _______.
As lacunas do texto devem ser preenchidas por:

(www.emsintese.com.br)
Nesse experimento, ocorre uma reação de oxirredução, na qual
Uma das maneiras de se obter industrialmente o hidrogênio é pelo processo conhecido como “reforma de hidrocarbonetos a vapor”, que envolve a reação entre hidrocarboneto e água no estado gasoso, gerando como produtos gasosos CO e H2 . Considere os valores das entalpias de formação indicados na tabela. Uma das maneiras de se obter industrialmente o hidrogênio é pelo processo conhecido como “reforma de hidrocarbonetos a vapor”, que envolve a reação entre hidrocarboneto e água no estado gasoso, gerando como produtos gasosos CO e H2 .
Considere os valores das entalpias de formação indicados na tabela.
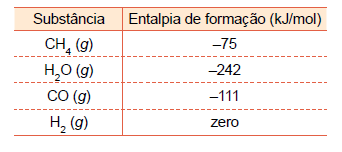
A partir das informações fornecidas, calcula-se que a produção
de cada mol de hidrogênio pela reforma a vapor do metano
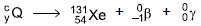
O radioisótopo
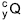 é inserido em cápsulas. Para realizar a
radioterapia, o paciente é isolado em instalação hospitalar
adequada onde ingere uma dessas cápsulas e permanece
internado até que a atividade do radioisótopo atinja valores
considerados seguros, o que ocorre após o tempo mínimo
correspondente a 3 meias-vidas do radioisótopo.
é inserido em cápsulas. Para realizar a
radioterapia, o paciente é isolado em instalação hospitalar
adequada onde ingere uma dessas cápsulas e permanece
internado até que a atividade do radioisótopo atinja valores
considerados seguros, o que ocorre após o tempo mínimo
correspondente a 3 meias-vidas do radioisótopo. A figura apresenta a curva de decaimento radioativo para
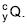
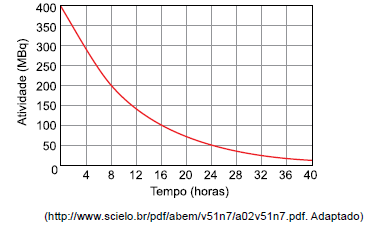
O radioisótopo
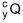 e o tempo mínimo que o paciente deve
permanecer internado e isolado quando é submetido a esse
tipo de radioterapia são, respectivamente,
e o tempo mínimo que o paciente deve
permanecer internado e isolado quando é submetido a esse
tipo de radioterapia são, respectivamente,I. C(graf) + O2(g) → CO2(g) ΔH°= – 394 kJ/mol
II. H2(g) + 1/2 O2(g) → H2O(ℓ) ΔH° = – 242 kJ/mol
III. C(graf) + 2 H2(g) → CH4(g) ΔH° = – 74 kJ/mol
IV. 2 C(graf) + 3 H2(g) + 1/2 O2(g) → C2H5OH(ℓ) ΔH° = – 278 kJ/mol
É correto afirmar que
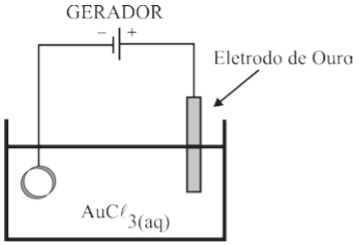
Dados: Au = 197 g/mol e 1 mol de elétrons = 9,6∙104 C.
A respeito do processo eletroquímico ilustrado acima, considere as afirmações dadas, de I a V.
I. O anel foi colocado no ânodo da cuba eletrolítica.
II. Ao passar uma corrente de 3 ampères, durante 16 minutos, há a deposição de aproximadamente 2,0 g de ouro sobre o anel.
III. No polo positivo ocorre a reação Au(s) → Au3+(aq) + 3 e-.
IV. No cátodo da cela eletrolítica ocorre oxidação.
V. No anel ocorre a reação Au3+(aq) + 3 e- → Au(s).
Dessas afirmações, estão corretas, somente
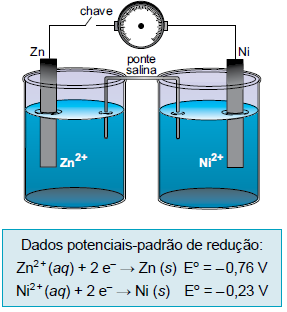
O catodo e a diferença de potencial da pilha são, respectivamente,